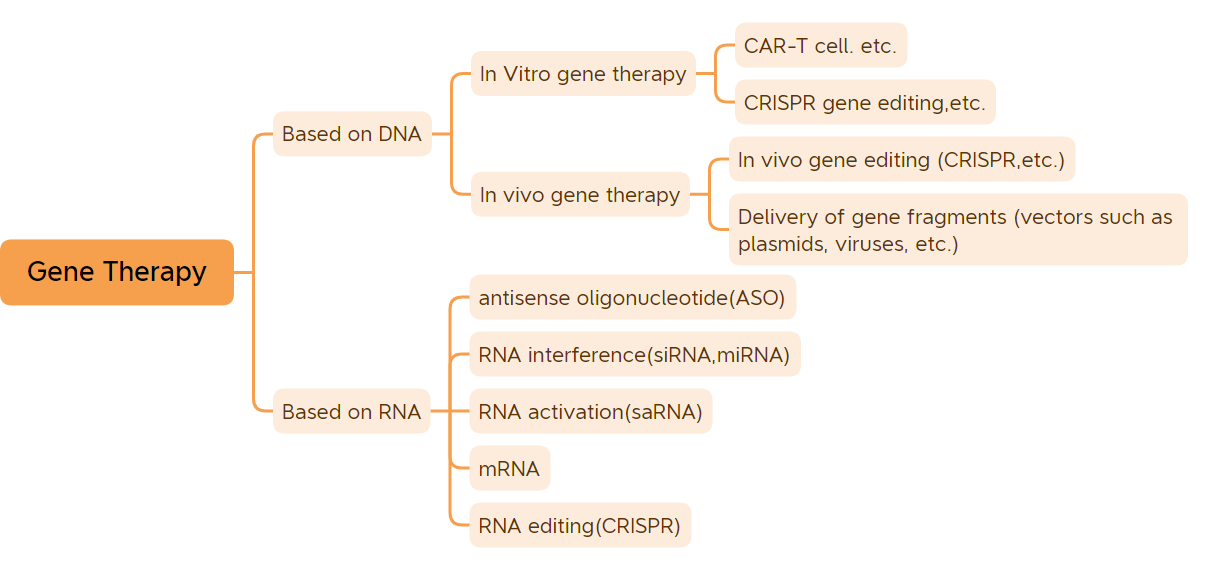
Gen yekîneyên genetîkî yên bingehîn in ku taybetmendiyan kontrol dikin.Ji xeynî genên hin vîrusan, ku ji ARNyê pêk tên, genên piraniya zîndeweran ji DNAyê pêk tên..Piraniya nexweşiyên zîndeweran ji têkiliya genan û jîngehê pêk tên.Terapiya genê bi bingehîn dikare gelek nexweşiyan qenc bike an sivik bike.Terapiya genê di warê derman û dermansaziyê de wekî şoreşek tê hesibandin.Dermanên tedawiya genê di wateyek berfireh de li ser bingeha dermanên DNA-yê guhertî (wek dermanên terapiya genê in vivo yên ku li ser vektorên vîrusê ne, dermanên terapiya genê in vitro, dermanên plasmîd ên tazî, hwd.) û dermanên RNA (wek dermanên oligonukleotîd ên antîsens, dermanên siRNA, û terapiya genê mRNA, hwd.) vedigirin.Dermanên terapiya genê bi giranî dermanên DNA-ya plazmidî, dermanên terapiya genê yên li ser vektorên vîrusê, dermanên terapiya genê yên li ser bingeha vektorên bakterî, pergalên guherandina genan, û dermanên terapiya hucreyê yên ji bo guheztina genê in vitro vedihewînin.Piştî salên pêşkeftina dijwar, dermanên terapiya genê encamên klînîkî yên teşwîq bi dest xistin.(Daşeyên DNA û derziyên mRNA nayê hesibandin) Niha li cîhanê 45 dermanên terapiya genê ji bo kirrûbirrê hatine pejirandin.Bi tevahî 9 dermanên genî îsal ji bo kirrûbirrê hatine pejirandin, di nav de 7 dermanên genî ji bo kirrûbirrê yekem car îsal hatine pejirandin, bi navî: CARVYKTI, Amvuttra, Upstaza, Roctavian, Hemgenix, Adstiladrin û Ebvallo, (Têbînî: Her duyên din îsal li Dewletên Yekbûyî hatin pejirandin. Yekem parê rapiesnteyê ku ji hêla DA-yê ve hatî pejrandin ji hêla ji bo kirrûbirra li Dewletên Yekbûyî di Tebaxa 2022 de, û ji bo kirrûbirrê ji hêla Yekîtiya Ewropî ve di sala 2019-an de hate pejirandin;
Dabeşkirina dermankirina genê (Çavkaniya wêneyê: Bio-Matrix)
Ev gotar 45 tedawiyên genê (ji bilî derziyên DNA û derziyên mRNA) yên ku ji bo kirrûbirrê hatine pejirandin navnîş dike.
1. Terapiya gene ya in vitro
(1) Strimvelis
Pargîdanî: Ji hêla GlaxoSmithKline (GSK) ve hatî pêşve xistin.
Dema bazarê: Ew ji bo kirrûbirrê ji hêla Yekîtiya Ewropî ve di Gulana 2016 de hate pejirandin.
Nîşan: Ji bo dermankirina kêmasiya hevgirtî ya giran (SCID).
Nîşe: Pêvajoya giştî ya vê terapiyê ew e ku pêşî şaneyên stem ên hematopoietic ên nexweş bi dest bixe, berfireh bike û wan di vitro de çand bike, piştre retrovirus bikar bîne da ku kopiyek genê ADA (adenosine deaminase) bikêrhatî bike nav hucreyên stem ên hematopoietîk, û di dawiyê de şaneyên bingehîn ên Hematopoetîk ên guhertî têne derzî kirin ku ji nû ve vedigerin laş.Encamên klînîkî destnîşan dikin ku rêjeya zindîbûna 3-salî ya nexweşên ADA-SCID yên ku bi Strimvelis têne derman kirin 100%.
(2) Zalmoxis
Pargîdanî: Ji hêla Italytalya MolMed Company ve hatî hilberandin.
Dema bazarê: Di sala 2016-an de destûrnameya kirrûbirra şertî ji Yekîtiya Ewropî wergirt.
Nîşan: Ji bo dermankirina alîkar a pergala parastinê ya nexweşan piştî veguheztina hucreyên stem ên hematopoietic tê bikar anîn.
Nîşan: Zalmoxis immunoterapiya genê xwekujî ya hucreya T alojenîk e ku ji hêla vektorên retroviral ve hatî guheztin.Ev rêbaz vektorên retroviral bikar tîne da ku bi rengek genetîkî şaneyên T alojenîk biguhezîne, ji ber vê yekê şaneyên T-yên guherbar ên genetîkî 1NGFR û HSV-TK Mut2 genên xwekuştinê diyar dikin ku mirov di her kêliyê de dermanên ganciclovir (ganciclovir) bikar bînin da ku hucreyên T yên ku dibin sedema reaksiyonên bêparastinê yên nebaş bikujin, pêşî li xirabûna ihtîmala ji nûvekirina nexweşên GV-yê, û fonksiyona ji nûvekirina nexweşan a HDS-ê vebikin t.
(3) Invossa-K
Pargîdanî: Ji hêla TissueGene (KolonTissueGene) ve hatî pêşve xistin.
Dema bazarê: Ji bo navnîşkirina li Koreya Başûr di Tîrmeha 2017 de hate pejirandin.
Nîşan: Ji bo dermankirina gewriya çokê dejeneratîf.
Nîşan: Invossa-K tedawiyek genê ya hucreya alojenîk e ku tê de chondrocytes mirovan pêk tîne.Hucreyên alojenîk in vitro bi genetîkî têne guheztin, û şaneyên guhezbar dikarin piştî derzîlêdana hundurîn-artikular faktora mezinbûnê β1 (TGF-β1) veguhezînin û derbixin.β1), bi vî rengî nîşanên osteoarthritis çêtir dike.Encamên klînîkî destnîşan dikin ku Invossa-K dikare bi girîngî gewriya çokê çêtir bike.Ew di sala 2019-an de ji hêla Rêvebiriya Xurek û Dermanê Koreyî ve hate betal kirin ji ber ku çêker malzemeyên ku hatine bikar anîn xelet nîşan kir.
(4) Zynteglo
Pargîdanî: Ji hêla bluebird bio ve hatî lêkolîn û pêşxistin.
Dema bazarê: Ji hêla Yekîtiya Ewropî ve ji bo kirrûbirra 2019-an ve hatî pejirandin, û ji hêla FDA ve ji bo kirrûbirra li Dewletên Yekbûyî di Tebaxa 2022-an de hate pejirandin.
Nîşan: Ji bo dermankirina β-talasemiya girêdayî transfuzyonê.
Nîşe: Zynteglo tedawiyek genê ya in vitro ya lentîviral e ku kopiyek fonksiyonel a gena β-globînê ya normal (genê βA-T87Q-globîn) dixe nav hucreyên stem ên hematopoietîkî ku ji nexweş bi vektorek lentiviral ve hatî girtin, û dûv re van şaneyên stem ên otolog ên nexweş ên ku bi genetîkî hatine guheztin ji nû ve vedihewîne.Dema ku nexweş xwedî genek βA-T87Q-globînê ya normal be, ew dikare proteîna normal HbAT87Q hilberîne, ku dikare bi bandor hewcedariya veguheztina xwînê kêm bike an ji holê rake.Ew tedawiyek yek-car e ku ji bo nexweşên 12 salî û mezintir li şûna veguheztina xwînê û dermanên heyata heyatê hatî çêkirin.
(5) Skysona
Pargîdanî: Ji hêla bluebird bio ve hatî lêkolîn û pêşxistin.
Dema bazarê: Ji hêla Yekîtiya Ewropî ve ji bo kirrûbirrê di Tîrmeha 2021-an de hate pejirandin, û ji hêla FDA ve ji bo kirrûbirra li Dewletên Yekbûyî di îlona 2022-an de hate pejirandin.
Nîşan: Ji bo dermankirina adrenoleukodystrophy ya mêjî ya zû (CALD).
Nîşan: Tedawiya genê Skysona tenê tedawiya genê ya yek-car e ku ji bo dermankirina adrenoleukodystrophy ya mêjî ya qonaxa destpêkê (CALD) hatî pejirandin.Skysona (elivaldogene autotemcel, Lenti-D) lentîviralek hucreya stem a hematopoietîkî ye ku di vitro dermankirina genê Lenti-D de ye.Pêvajoya giştî ya dermankirinê wiha ye: Hucreyên stem ên hematopoietîkî yên xweser ji nexweş têne derxistin, ji hêla lentivirus ve ku gena mirovî ABCD1 in vitro hildigire, têne veguheztin û guheztin û paşê ji nû ve vedigerin nexweş.Ew ji bo dermankirina nexweşên di bin 18 saliyê de, ku mutasyonên genê ABCD1, û CALD hildigirin, tê bikar anîn.
(6) Kymriah
Şîrket: Ji hêla Novartis ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Tebaxa 2017 de hate pejirandin.
Nîşan: Dermankirina leukemiya lîmfoblastîk a akût a hucreya B (ALL) û DLBCL ya paşveçûyî û refraktor.
Nîşan: Kymriah dermanek dermankirina genê ya in vitro ya lentiviral e, yekem terapiya CAR-T ku ji bo kirrûbirrê li cîhanê hatî pejirandin, CD19 armanc dike, û faktora hev-stimulatorê 4-1BB bikar tîne.Bihayê wê li Dewletên Yekbûyî 475,000 dolar û li Japonya 313,000 dolar e.
(7) Yescarta
Pargîdanî: Ji hêla Kite Pharma, pargîdaniyek Gilead (GILD) ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Cotmeha 2017-an de hate pejirandin;Fosun Kite teknolojiya Yescarta ji Kite Pharma destnîşan kir û piştî wergirtina destûrnameyê li Chinaînê hilberand.Ji bo navnîşê li welat hate pejirandin.
Nîşan: Ji bo dermankirina lîmfoma şaneyên B-ya mezin a paşveçûyî an jî refraktor.
Nîşan: Yescarta tedawiyek genê in vitro ya retroviral e, ku duyemîn tedawiya CAR-T ya pejirandî ye li cîhanê.Ew CD19 armanc dike û kostimulatorê CD28 qebûl dike.Bihayê wê li Dewletên Yekbûyî $373,000 e.
(8) Tecartus
Pargîdanî: Ji hêla Gilead (GILD) ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Tîrmeha 2020-an de hate pejirandin.
Nîşan: Ji bo lîmfoma xaneyên mantoyê yên paşveçûyî an jî refraktor.
Nîşan: Tecartus tedawiyek hucreya CAR-T ya xweser e ku CD19 armanc dike, û ew sêyemîn terapiya CAR-T ye ku ji bo kirrûbirrê li cîhanê hatî pejirandin.
(9) Breyanzi
Şîrket: Ji hêla Bristol-Myers Squibb (BMS) ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Sibata 2021-an de hate pejirandin.
Nîşan: Lenfomaya B-hucreya B ya mezin (LBCL) ya paşveçûyî an jî refraktor (R/R).
Nîşan: Breyanzi tedawiyek genê in vitro ye ku li ser bingeha lentivirus e, çaremîn terapiya CAR-T ku ji bo kirrûbirra li cîhanê hatî pejirandin, CD19 armanc dike.Pejirandina Breyanzi ji bo Bristol-Myers Squibb di warê immunoterapiya hucreyî de, ku ew di sala 2019-an de Celgene bi 74 mîlyar dolarî bi dest xist, qonaxek e.
(10) Abecma
Pargîdanî: Ji hêla Bristol-Myers Squibb (BMS) û biyo bluebird ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Adara 2021-an de hate pejirandin.
Nîşan: myeloma piralî ya paşveçûyî an jî refraktor.
Nîşan: Abecma tedawiyek genê ya in vitro ye ku li ser bingeha lentivirus e, yekem tedawiya hucreya CAR-T ya cîhanê ku BCMA armanc dike, û tedawiya CAR-T ya pêncemîn ku ji hêla FDA ve hatî pejirandin.Prensîba derman ev e ku receptorên BCMA yên chimerîk li ser hucreyên T yên nexweş bi navbeynkariya lentivirus-guheztina genê di vitro de diyar bike.Dermankirin ji bo rakirina şaneyên T-yên ne-genetîkî yên ne-guhartî yên di nexweşan de, û dûv re şaneyên T-yên guhezbar ên ku di nexweşan de şaneyên penceşêrê yên BCMA-ê diyar dikin digerin û dikujin.
(11) Libmeldy
PARTIYA: Ji hêla Orchard Therapeutics ve hatî pêşve xistin.
Dema bazarê: Ji hêla Yekîtiya Ewropî ve ji bo navnîşê di Kanûna 2020-an de hate pejirandin.
Nîşan: Ji bo dermankirina leukodystrophy metachromatic (MLD).
Nîşan: Libmeldy tedawiyek genê ye ku li ser hucreyên CD34+ yên xweser ên ku bi genetîkî ve di vitro de ji hêla lentivirus ve hatî guheztin, bingeh e.Daneyên klînîkî destnîşan dikin ku înfuzyonek intravenous a yekane ya Libmeldy dikare bi bandorkerî qursa MLD-ya zû-destpêkirî li gorî kêmbûna giran a motor û cognitive di nexweşên heman temenî de ku nehatine derman kirin biguhezîne.
(12) Benoda
Pargîdanî: Ji hêla WuXi Giant Nuo ve hatî pêşve xistin.
Demê bazarê: Bi fermî ji hêla NMPA ve di îlona 2021-an de hate pejirandin.
Nîşan: Dermankirina nexweşên mezin ên bi lîmfomaya B-hucreya mezin a vegerandî an refraktor (r/r LBCL) piştî dermankirina pergalê ya rêza duyemîn an jorîn.
Nîşan: Beinoda tedawiyek genê ya dijî CD19 CAR-T ye, û ew di heman demê de hilbera bingehîn a Pargîdaniya WuXi Juro ye.Ew duyemîn hilbera CAR-T ye ku li Chinaînê hatî pejirandin, ji xeynî lîmfoîdeya B-hucreya B-ya mezin a paşveçûn/rengdêr WuXi Giant Nuo di heman demê de plan dike ku derzîlêdana Regiorensai ji bo dermankirina gelek nîşanên din jî pêş bixe, di nav de lîmfoma folîkular (FL), lîmfoma hucreya mantoyê (MCL), lemphozeya kronîk (lîmphosiya mezin a kronîk-CLL) DLBCL) û leukemia lîmfoblastîk a akût (ALL).
(13) CARVYKTI
Pargîdanî: Yekem hilbera Legend Biotech ji bo kirrûbirrê hatî pejirandin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Sibata 2022-an de hate pejirandin.
Nîşan: ji bo dermankirina mîeloma piralî ya paşveçûyî an refraktor (R/R MM).
Nîşan: CARVYKTI (ciltacabtagene autoleucel, bi kurtasî Cilta-cel) tedawiyek genê nepenî ya hucreya CAR-T ye ku bi du antîbodên yek-domînê re antîjena mezinbûna hucreya B (BCMA) hedef digire.Daneyên nîşan didin ku CARVYKTI Di nexweşên bi mîeloma piralî ya paşveçûyî an refraktîf de ku çar an bêtir dermanên berê wergirtine (di nav de înhîbîtorên proteazomê, immunomodulator û antî-CD38 antîbodîyên monoklonal jî hene), rêjeya bersivê ya giştî 98% hate destnîşan kirin.
(14)Ebvallo
PARTIYA: Ji hêla Atara Biotherapeutics ve hatî pêşve xistin.
Komîsyona Ewropî (EC) ji bo kirrûbirrê di Kanûna 2022-an de, ew yekem terapiya hucreya T-ya gerdûnî ya cîhanê ye ku ji bo kirrûbirrê hatî pejirandin.
Nîşan: Wek monoterapî ji bo nexweşiya lîmfoprolîferatîf a piştî veguheztinê (EBV+PTLD) bi vîrûsa Epstein-Barr (EBV) ve girêdayî ye, nexweşên ku têne derman kirin divê mezin û zarokên ji 2 salî mezintir bin ku berê bi kêmî ve dermanek dermanek din wergirtine.
Nîşan: Ebvallo tedawiyek genê-hucreya T-ya gerdûnî ya alojenîk a EBV-taybetî ye ku hucreyên enfeksiyonê yên EBV bi rengek HLA-sînorkirî hedef digire û ji holê radike.Pejirandina vê terapiyê li ser bingeha encamên lêkolîna ceribandina klînîkî ya qonaxa bingehîn 3 ye, û encaman destnîşan kir ku ORR ya koma HCT û koma SOT% 50 bû.Rêjeya bexşandina tam (CR) 26.3%, rêjeya bexşandina qismî (PR) 23.7%, û dema navînî bervebûnê (TTR) 1.1 meh bû.Ji 19 nexweşên ku remîsyonê bi dest xistin, 11 ji wan ji 6 mehan zêdetir maweya bersivê (DOR) bûn.Wekî din, di warê ewlehiyê de, ti reaksiyonên neyînî yên wekî nexweşiya graftî-li hember-mêvandar (GvHD) an sendroma serbestberdana cytokine-girêdayî Ebvallo pêk nehat.
2. Terapiya gene ya in vivo ya li ser vektorên vîrusê
(1) Jendîsîn/Jin Şeng
Pargîdanî: Ji hêla Şirketa Shenzhen Saibainuo ve hatî pêşve xistin.
Dema bazarê: Pejirandin ku di sala 2003-an de li Chinaînê were navnîş kirin.
Nîşan: Ji bo tedawiya kansera hucreya squamous ya ser û stûyê.
Nîşe: Derziya adenovirus a p53 ya mirovî ya rekombînant Gendicine/Jinyousheng dermanek dermankirina genê vektorê adenovirus e ku xwediyê mafên xwedan rewşenbîriya serbixwe ye ku xwediyê pargîdaniya Shenzhen Saibainuo ye.Adenovîrûsên mirovî 5 ji adenovîrûsên mirovî yên celeb 5 pêk tê. Ya yekem avahiya bingehîn e ji bo bandora dij-tumor a dermanê, û ya paşîn bi giranî wekî hilgirek tevdigere.Vektora adenovirus gena dermanker p53 di nav şaneya armancê de vedigire, di hucreya armancê de gena tepiskerê p53 ya tumorê derdixe holê, û îfadeya genê wê hilber dikare cûrbecûr genên dij-penceşêrê sererast bike û çalakiyên cûrbecûr onkojenan kêm bike, bi vî rengî bandora laş a tunekirina tumorê zêde bike û bikuje.
(2) Rigvir
Pargîdanî: Ji hêla Latima Company, Letonya ve hatî pêşve xistin.
Dema navnîşkirinê: Ji bo navnîşê li Letonya di 2004 de hate pejirandin.
Nîşan: Ji bo dermankirina melanoma.
Têbînî: Rigvir tedawiyek genê ye ku li ser vektorek enterovirus ECHO-7 bi genetîkî veguherî ye.Heya nuha, derman li Letonya, Estonya, Polonya, Ermenistan, Belarus, hwd., û li welatên Yekîtiya Ewropî jî di nav qeydkirina EMA de derbas dibe.Bûyerên klînîkî yên di deh salên borî de îsbat kirine ku vîrusa onkolîtîk Rigvir ewledar û bi bandor e, û dikare rêjeya zindîbûna nexweşên melanomayê 4-6 carî zêde bike.Wekî din, ev derman ji bo cûrbecûr penceşêrên din jî tê sepandin, di nav de kansera kolorektal, kansera pankreasê, kansera mîzê Penceşêrê, kansera gurçikê, kansera prostatê, kansera pişikê, kansera uterus, lymphosarcoma, hwd.
(3) Oncorine
Pargîdanî: Ji hêla Pargîdaniya Biyolojîkî ya Shanghai Sanwei ve hatî pêşve xistin.
Dema bazarê: Pejirandin ku di sala 2005-an de li Chinaînê were navnîş kirin.
Nîşan: dermankirina tumorên ser û stûyê, kansera kezebê, penceşêra pankreasê, kansera malzarokê û penceşêrên din.
Nîşe: Oncorine (安科瑞) hilberek tedawiya genê ya virusê onkolîtîk e ku adenovirus wekî hilgirê bikar tîne.Adenovîrûsek onkolîtîk tê peyda kirin, ku dikare bi taybetî di tumorên kêmasiya genê p53 an anormal de dubare bibe, ku bibe sedema lîza hucreyên tumor, bi vî rengî hucreyên tumorê bikuje.bêyî ku zirarê bide şaneyên normal.Lêkolînên klînîkî destnîşan kirin ku Ankerui ji bo cûrbecûr tîmorên nebaş xwedî ewlehî û bandorek baş e.
(4) Glybera
Pargîdanî: Ji hêla uniQure ve hatî pêşve xistin.
Demjimêra bazarê: Di sala 2012-an de ji bo navnîşkirina li Ewrûpayê hate pejirandin.
Nîşan: Dermankirina kêmbûna lîpoproteîn lîpazê (LPLD) bi serpêhatiyên giran an dûbareyî yên pankreatîtê re tevî parêzek rûnê ya hişk a sînorkirî.
Nîşan: Glybera (alipogene tiparvovec) dermanek terapiya genê ye ku li ser bingeha AAV-ê ye, ku AAV-ê wekî hilgirek bikar tîne da ku gena dermanker LPL di nav şaneyên masûlkan de veguhezîne, da ku şaneyên têkildar karibin hejmareke diyarkirî ya lîpoproteîn lipase hilberînin.Derman di sala 2017-an de ji bazarê hate derxistin. Dibe ku sedema vekişîna wê bi du faktoran ve girêdayî be: nirxa bilind û daxwaziya bazarê ya sînorkirî.Lêçûna dermankirinê ya navînî ya derman bi qasî 1 mîlyon dolar e, û tenê nexweşek heya nuha ew kirî û bikar aniye.Tevî ku şirketa bîmeya pijîşkî 900,000 dolarên Amerîkî ji bo wê vegerandiye, ew jî bargiraniyek mezin e ji bo pargîdaniya bîmeyê.Wekî din, nîşanên ku ji hêla derman ve têne armanc kirin pir kêm in, bi rêjeya bûyera li ser 1 mîlyon û rêjeyek bilind a teşhîsa xelet.
(5) Imlygic
Pargîdanî: Ji hêla Amgen ve hatî pêşve xistin.
Dema bazarê: Di 2015 de, ew hate pejirandin ku li Dewletên Yekbûyî û Yekîtiya Ewropî were navnîş kirin.
Nîşan: Dermankirina birînên melanoma ku bi emeliyatê bi tevahî nayên rakirin.
Nîşe: Imlygic vîrusek herpes simplex a tîpa 1 ya qelskirî ye ku ji hêla teknolojiya genetîkî ve hatî guheztin (parçeyên genê yên ICP34.5 û ICP47 jêbirin, û gena faktora GM-CSF a koloniya granulocît a mirovî têxe nav vîrusê) (HSV-1 bi vîrusa FDA-genetîk ve pêşî li terapiya vîrusê tête pejirandin.Rêbaza rêvebirinê derzîlêdana hundurîn e, ku dikare rasterast di birînên melanoma de were derzî kirin da ku bibe sedema şikestina hucreyên tumor, berdana antîjenên ji tumor û GM-CSF, û pêşvebirina bersivên berevaniyê yên dijî-tumor.
(6) Luxturna
Pargîdanî: Ji hêla Spark Therapeutics, pargîdaniyek Roche ve hatî pêşve xistin.
Dema bazarê: Ew ji bo kirrûbirrê ji hêla FDA ve di sala 2017-an de hate pejirandin, û dûv re ji bo kirrûbirra li Ewrûpa di 2018-an de hate pejirandin.
Nîşan: Ji bo dermankirina zarok û mezinên ku ji ber mutasyonên genê RPE65 du-kopî dîtinê winda kirine, lê hejmarek têr şaneyên retînal ên zindî diparêzin.
Nîşe: Luxturna tedawiyek genê ya AAV-ê ye ku bi derziya subretinal ve tê rêve kirin.Terapiya genê AAV2 wekî hilgirê bikar tîne da ku kopiyek fonksiyonel a gena RPE65 ya normal bikeve nav hucreyên retînal ên nexweş, da ku şaneyên têkildar proteîna RPE65 ya normal îfade bikin, kêmbûna proteîna RPE65 ya nexweş çêbike, bi vî rengî dîtina nexweş baştir dike.
(7) Zolgensma
Pargîdanî: Ji hêla AveXis, pargîdaniyek Novartis ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Gulana 2019-an de hate pejirandin.
Nîşan: Dermankirina nexweşên di bin 2 salî de Atrofiya Muskuler a Spinal (SMA).
Têbînî: Zolgensma tedawiyek genê ye ku li ser vektorê AAV-ê ye.Ev derman yekane plana dermankirinê ya yek-car e ji bo atrofiya masûlkeya spî ya ku ji bo kirrûbirrê li cîhanê hatî pejirandin.Destpêkirina dermanê di dermankirina atrofiya masûlkeya spî de serdemek nû vedike.rûpel, pêşveçûnek qonaxek e.Vê terapiya genê vektora scAAV9 bikar tîne da ku gena normal SMN1 bi navgîniya înfuzyonê ya hundurîn ve bide nav nexweş da ku proteîna SMN1 ya normal hilberîne, bi vî rengî fonksiyona şaneyên bandorkirî yên wekî neuronên motorê baştir dike.Berevajî vê, dermanên SMA Spinraza û Evrysdi hewceyê dozek dubare ya dirêj-dirêj hewce dike.Spinraza her çar mehan carekê bi derziyê spinal tê dayîn, û Evrysdi dermanek devkî ya rojane ye.
(8) Delytact
Pargîdanî: Ji hêla Daiichi Sankyo Company Limited (TYO: 4568) ve hatî pêşve xistin.
Wexta bazarê: Pejirandina şertî ji Wezareta Tenduristî, Ked û Refahê ya Japonya (MHLW) di Hezîrana 2021-an de.
Nîşan: Ji bo dermankirina glioma ya xerab.
Nîşan: Delytact çaremîn hilbera dermankirina genê virusê onkolîtîk e ku li gerdûnî hatî pejirandin, û yekem hilbera virusê onkolîtîk e ku ji bo dermankirina glioma xirab hatî pejirandin.Delytact vîrusek herpes simplex a cureya 1 (HSV-1) ya bi endezyariya genetîkî ye ku ji hêla Dr. Todo û hevkarên wî ve hatî pêşve xistin.Delytact mutasyonên jêbirinê yên zêde dixe nav genoma G207-a nifşê duyemîn HSV-1, dubarekirina wê ya bijartî di hucreyên penceşêrê de zêde dike û di heman demê de ewlehiya bilind diparêze bersivên berevaniya dijî-tumor zêde dike.Delytact yekem-nifşa sêyemîn onkolîtîk HSV-1 e ku niha di bin nirxandina klînîkî de ye.Pejirandina Delytact li Japonya bi giranî li ser bingeha ceribandinek klînîkî ya qonaxa 2-ya yek-dest e.Di nexweşên bi glioblastoma dûbare de, Delytact xala dawî ya bingehîn a rêjeya zindîbûna yek-salî bi dest xist, û encaman destnîşan kir ku Delytact li gorî G207-ê çêtir bandorek nîşan da.Hêza dubarekirinê ya bihêz û çalakiya antîtumor ya bilind.Ev di modelên tîmora zexm ên pêsîrê, prostat, schwannomas, nasopharyngeal, hepatocellular, kolorektal, tumorên kelûpelên nerva periferîkî yên xerab, û kansera tîrîdê de bi bandor bû.
(9) Upstaza
PARTIYA: Ji hêla PTC Therapeutics, Inc. (NASDAQ: PTCT) ve hatî pêşve xistin.
Dema bazarê: Ji hêla Yekîtiya Ewropî ve ji bo kirrûbirrê di Tîrmeha 2022-an de hate pejirandin.
Nîşan: Ji bo kêmbûna L-amino acid decarboxylase (AADC) aromatic, ew ji bo dermankirina nexweşên 18 mehî û mezintir tê pejirandin.
Nîşe: Upstaza™ (eladocagene exuparvovec) tedawiyek genê di vivo de ye ku bi vîrusa adeno-girêdayî celeb 2 (AAV2) wekî hilgirê wê ye.Nexweş ji ber mutasyonên gena ku enzîma AADC kod dike nexweş dibin.AAV2 genek tendurist hildigire ku enzîma AADC kod dike.Forma tezmînata genê bandorek dermankirinê bi dest dixe.Di teoriyê de, yek rêveberî ji bo demek dirêj ve bandor e.Ew yekem terapiya genê ya bazarê ye ku rasterast di mêjî de tê derzî kirin.Destûrnameya kirrûbirrê ji bo hemî 27 welatên endamên Yekîtiya Ewropî, û her weha Îzlanda, Norwêc û Liechtenstein jî derbasdar e.
(10) Roktawî
Pargîdanî: Ji hêla BioMarin Pharmaceutical (BioMarin) ve hatî pêşve xistin.
Dema bazarê: Ji bo kirrûbirrê ji hêla Yekîtiya Ewropî ve di Tebaxa 2022-an de hate pejirandin;destûrnameya kirrûbirrê ji hêla Rêveberiya Derman û Hilberên Tenduristî ya Keyaniya Yekbûyî (MHRA) di Mijdara 2022-an de.
Nîşan: Ji bo dermankirina nexweşên mezin ên bi hemofîliya A-ya giran a ku dîroka wan a astengkirina faktora FVIII tune ye û ji bo antîkorên AAV5 neyînî ne.
Nîşan: Roctavian (valoctocogene roxaparvovec) AAV5 wekî vektorek bikar tîne û promotor-a kezeba-taybetî ya mirovî HLP bikar tîne da ku îfadeya faktora koagulasyona mirovî VIII (FVIII) bi qada B jêbirin.Biryara Komîsyona Ewropî ya pejirandina kirrûbirra valoctocogene roxaparvovec li ser bingeha daneyên giştî yên projeya pêşkeftina klînîkî ya dermanê ye.Di nav wan de, encamên ceribandina klînîkî ya qonaxa III GENER8-1 destnîşan kir ku li gorî daneyên salek beriya qeydkirinê, piştî yek înfuzyonek valoctocogene roxaparvovec, rêjeya xwînê ya salane ya mijarê (ABR) bi girîngî kêm dibe, pirbûna karanîna faktora koagulasyona rekombînant VIII (F8) di amadekariyên proteîn ên laş de di laş de girîng kêm dibe an jî çalakiya proteîna xwînê ya F8 girîng kêm dibe.Piştî 4 hefteyên dermankirinê, rêjeya karanîna salane ya F8 û ABR ya ku hewceyê dermankirinê ye, bi rêzê ve ji sedî 99% û 84% kêm bû, û cûdahî ji hêla statîstîkî ve girîng bû (p<0.001).Profîla ewlehiyê baş bû, û tu mijarek nehiştina faktora F8, bandorên alîgirê xirabûnî an trombozê, û bûyerên neyînî yên cidî yên girêdayî dermankirinê (SAE) nehatin rapor kirin.
(11) Hemgenix
Pargîdanî: Ji hêla Pargîdaniya UniQure ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Mijdara 2022-an de hate pejirandin.
Nîşan: Ji bo dermankirina nexweşên mezin ên bi hemofîliya B.
Têbînî: Hemgenix tedawiyek genê ye ku li ser vektora AAV5-ê ye.Derman bi guhertoya genê ya faktora koagulasyonê IX (FIX) FIX-Padova ve girêdayî ye, ku bi hundurê venoz ve tête bikar anîn.Piştî rêveberiyê, gen dikare di kezebê de faktora koagulasyonê ya FIX eşkere bike û derxe.
(12) Adstiladrin
Pargîdanî: Ji hêla Ferring Pharmaceuticals ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Kanûna 2022-an de hate pejirandin.
Nîşan: Ji bo dermankirina kansera mîzdankê ya ne-masûlke-dagirker (NMIBC) ya bi rîska bilind ku bersivê nade Bacillus Calmette-Guerin (BCG).
Nîşan: Adstiladrin tedawiyek genê ye ku li ser vektorek adenovîral a ne-berhevkirî ye, ku dikare proteîna înterferon alfa-2b di hucreyên armanc de zêde derbixe, û bi kateterek mîzê di mîzê de tê rêve kirin (her sê mehan carekê tê rêvebirin), vektora vîrusê dikare bi bandor li şaneyên dîwarê mîzdankê bi bandor bike û dûv re jî bandorek proteîn2 bike. .Ev rêbaza terapiya genê ya nû bi vî rengî şaneyên dîwarê mîzê yê nexweş vediguherîne "fabrîkek" piçûk a ku înterferonê hildiberîne, bi vî rengî şiyana nexweş a şerkirina penceşêrê zêde dike.
Ewlehî û bandorkeriya Adstiladrin di lêkolînek klînîkî ya pir-navendî de ku tê de 157 nexweşên bi xetereya bilind a BCG-nebersiv NMIBC tê de hate nirxandin.Nexweşan her sê mehan carekê Adstiladrin distînin heya 12 mehan, an heya ku jehrîbûnek neyê pejirandin ji bo dermankirinê an dubarebûna NMIBC-a pola bilind.Bi tevayî, ji sedî 51 ê nexweşên qeydkirî yên ku bi Adstiladrin re têne derman kirin bersivek bêkêmasî bi dest xistin (wendabûna hemî nîşanên penceşêrê ku li ser cystoscopy, tevnek biopsî û mîzê têne dîtin).
3. Dermanên asîda nukleîk ên piçûk
(1) Vitravene
Pargîdanî: Ji hêla Ionis Pharma (berê Isis Pharma) û Novartis ve hatî pêşve xistin.
Dema bazarê: Di 1998 û 1999 de, ew ji hêla FDA û EU EMA ve ji bo kirrûbirrê hate pejirandin.
Nîşan: Ji bo dermankirina retinitis cytomegalovirus di nexweşên HIV-erênî de.
Nîşan: Vitravene dermanek oligonukleotîdê antîsens e, ku yekem dermanê oligonukleotîd e ku ji bo kirrûbirrê li cîhanê hatî pejirandin.Di qonaxa destpêkê ya navnîşkirinê de, daxwaza bazarê ji bo dermanên dijî-CMV pir bilez bû;paşê, ji ber pêşkeftina dermankirina antîretroviral a pir çalak, hejmara bûyerên CMV bi tundî daket.Ji ber kêmbûna daxwaziya bazarê, derman di 2002 û 2006 de vekişîna li welatên Yekîtiya Ewropî û Dewletên Yekbûyî hate destpêkirin.
(2) Macugen
Pargîdanî: Ji hêla Pfizer û Eyetech ve hatî pêşve xistin.
Demjimêra bazarê: Di sala 2004-an de ji bo navnîşkirina Dewletên Yekbûyî hate pejirandin.
Nîşan: Ji bo dermankirina dejenerasyona makûl a bi temenê neovaskuler.
Nîşan: Macugen dermanek oligonukleotîdê guhezbar a pegylated e, ku dikare faktora mezinbûna endotelyal a vaskal (bincûreya VEGF165) armanc bike û girêde, û rêbaza rêveberiyê derzîlêdana intravîtreal e.
(3) Defitelio
Pargîdanî: Ji hêla Jazz Pharmaceuticals ve hatî pêşve xistin.
Dema bazarê: Ew ji bo kirrûbirrê ji hêla Yekîtiya Ewropî ve di 2013-an de hate pejirandin û ji hêla FDA ve ji bo kirrûbirrê di Adara 2016-an de hate pejirandin.
Nîşan: Ji bo dermankirina nexweşiya veno-oklusive ya kezebê ya ku bi xerabûna renal an pişikê ve girêdayî ye piştî veguheztina şaneyên stem ên hematopoietic.
Têbînî: Defitelio dermanek oligonukleotîd e, ku tevliheviyek ji oligonukleotîdên bi taybetmendiyên plazmînê ye.Di 2009 de ji ber sedemên bazirganî ji bazarê vekişand.
(4) Kynamro
Pargîdanî: Ji hêla Ionis Pharma û Kastle ve hatî pêşve xistin.
Dema bazarê: Di 2013 de, ew ji bo kirrûbirra li Dewletên Yekbûyî wekî dermanek sêwî hate pejirandin.
Nîşan: Ji bo dermankirina alîkar a hîperkolesterolemiya malbatî ya homozîgot.
Nîşan: Kynamro dermanek oligonukleotîdek antîsens e, ku oligonukleotîdek antîsens e ku apo B-100 mRNAya mirovî dike hedef.Kynamro wekî 200 mg di bin çerm de hefteyek carekê tê bikar anîn.
(5) Spinraza
Pargîdanî: Ji hêla Ionis Pharmaceuticals ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Kanûna 2016-an de hate pejirandin.
Nîşan: Ji bo dermankirina atrofiya masûlkeya spinal (SMA).
Têbînî: Spinraza (nusinersen) dermanek oligonukleotîdê antîsens e.Bi girêdana bi cîhê veqetandina SMN2 exon 7, Spinraza dikare perçebûna RNA ya gena SMN2 biguhezîne, bi vî rengî hilberîna proteîna SMN ya bi tevahî fonksiyonel zêde bike.Di Tebaxa 2016-an de, BIOGEN vebijarka xwe ji bo bidestxistina mafên gerdûnî yên Spinraza bikar anî.Spinraza tenê di sala 2011-an de ceribandina xweya klînîkî ya yekem di mirovan de dest pê kir. Tenê di 5 salan de, ew di sala 2016-an de ji hêla FDA ve ji bo kirrûbirrê hate pejirandin, ku ev yek bi tevahî nasîna FDA ya bandoriya wê nîşan dide.Derman ji bo kirrûbirra li Chinaînê di Nîsana 2019-an de hate pejirandin. Tevahiya çerxa pejirandinê ya Spinraza li Chinaînê ji 6 mehan kêmtir bû, û ji ber ku Spinraza yekem car li Dewletên Yekbûyî hate pejirandin 2 sal û 2 meh derbas bûn.Leza navnîşkirina li Chinaînê jixwe pir bilez e.Ev jî ji ber wê yekê ye ku Navenda Nirxandina Dermanan di 1ê Mijdara 2018an de "Agahdariya li ser Weşandina Lîsteya Yekem Dermanên Nû yên Derve yên Dermanên Nû ku Bi Lezgînî Di Pratîka Klînîkî de Pêwîst e" derxist û di beşa yekem a 40 dermanên nû yên biyanî de ji bo vekolîna bilez hat girtin, ku di nav wan de Spinza rankedra bû.
(6) Exondys 51
Pargîdanî: Ji hêla AVI BioPharma ve hatî pêşve xistin (paşê navê Sarepta Therapeutics hate guherandin).
Dema bazarê: Di îlona 2016 de, ew ji hêla FDA ve ji bo kirrûbirrê hate pejirandin.
Nîşan: Ji bo dermankirina dîstrofiya masûlkeya Duchenne (DMD) bi exon 51 mutasyona genê ya di gena DMD de derbas dibe.
Nîşan: Exondys 51 dermanek oligonukleotîdê antîsens e, oligonucleotide antîsens dikare bi pozîsyona exon 51 ya pre-mRNA ya gena DMD ve girê bide, di encamê de mRNAya gihîştî çêdibe, beşek ji exon 51 tê asteng kirin. proteîna normal, bi vî rengî nîşanên nexweş çêtir dike.
(7) Tegsedî
Pargîdanî: Ji hêla Ionis Pharmaceuticals ve hatî pêşve xistin.
Dema bazarê: Ew ji bo kirrûbirrê ji hêla Yekîtiya Ewropî ve di Tîrmeha 2018-an de hate pejirandin.
Nîşan: Ji bo dermankirina amyloidosis transthyretin irsî (hATTR).
Nîşan: Tegsedi dermanek oligonukleotîdê antîsens e ku mRNAya transthyretin armanc dike.Ew yekem derman e ku di cîhanê de ji bo dermankirina hATTR hatî pejirandin.Ew bi derzîlêdana binê çermê tê rêvebirin.Derman hilberîna proteîna ATTR bi hedefgirtina mRNA ya transthyretin (ATTR) kêm dike, û di dermankirina ATTR de xwedan rêjeyek berjewendî-rîskek baş e, û neuropatî û kalîteya jiyanê ya nexweş bi giranî baştir bûye, û ew bi celebên mutasyona TTR re hevaheng e, Ne qonaxa nexweşiyê û ne jî hebûna kardiomiopatiyê têkildar bû.
(8) Onpattro
Pargîdanî: Ji hêla Alnylam Corporation û Sanofi Corporation ve bi hev re hatî pêşve xistin.
Dema bazarê: Ji bo navnîşa Dewletên Yekbûyî di sala 2018 de hate pejirandin.
Nîşan: Ji bo dermankirina amyloidosis transthyretin irsî (hATTR).
Nîşan: Onpattro dermanek siRNA ye ku mRNAya transthyretin armanc dike, ku hilberîna proteîna ATTR di kezebê de kêm dike û berhevkirina depoyên amyloid di nervên periferîkî de bi armanckirina mRNA ya transthyretin (ATTR) kêm dike, bi vî rengî nîşanên nexweşiyê baştir û sivik dike.
(9) Givlaari
Pargîdanî: Ji hêla Alnylam Corporation ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Mijdara 2019-an de hate pejirandin.
Nîşan: Ji bo dermankirina porfîriya kezebê ya akût (AHP) di mezinan de.
Nîşan: Givlaari dermanek siRNA ye, ku duyemîn dermanê siRNA ye ku piştî Onpattro ji bo kirrûbirrê hatî pejirandin.Awayê rêvebirinê derzîlêdana binê çerm e.Derman mRNA ya proteîna ALAS1 armanc dike, û dermankirina mehane ya bi Givlaari dikare bi girîngî û domdarî asta ALAS1 di kezebê de kêm bike, bi vî rengî asta neurotoksîk ALA û PBG di asta normal de kêm bike, bi vî rengî nîşanên nexweşiya nexweş kêm bike.Daneyan destnîşan kir ku nexweşên ku bi Givlaari re têne derman kirin ji sedî 74 kêmbûnek di hejmara stendinê de li gorî koma placebo heye.
(10) Vyondys53
COMPANY: Ji hêla Sarepta Therapeutics ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Kanûna 2019-an de hate pejirandin.
Nîşan: Ji bo dermankirina nexweşên DMD yên bi mutasyona splicing exon 53 gene dystrophin.
Nîşan: Vyondys 53 dermanek oligonukleotîdê antîsens e, ku pêvajoya veqetandina dîstrofîn a pre-mRNA armanc dike.Exon 53 bi qismî qutkirî ye, ango li ser mRNAya gihîştî tune ye, û ji bo hilberîna dîstrofînek qutkirî lê hîn fonksiyonel e, bi vî rengî kapasîteya werzîşê ya nexweşan baştir dike.
(11) Waylivra
Pargîdanî: Ji hêla Ionis Pharmaceuticals û pargîdaniya wê Akcea Therapeutics ve hatî pêşve xistin.
Dema bazarê: Ew ji bo kirrûbirrê ji hêla Ajansa Dermanên Ewropî (EMA) di Gulana 2019-an de hate pejirandin.
Nîşan: Wekî tedawiyek alîkar ji bilî kontrolkirina parêzê li nexweşên mezin ên bi sendroma chylomicronemia malbatî (FCS).
Nîşan: Waylivra dermanek oligonukleotîd a antîsens e, ku yekem derman e ku ji bo kirrûbirra li cîhanê ji bo dermankirina FCS hatî pejirandin.
(12) Leqvio
Pargîdanî: Ji hêla Novartis ve hatî pêşve xistin.
Dema bazarê: Ji hêla Yekîtiya Ewropî ve ji bo kirrûbirrê di Kanûna 2020-an de hate pejirandin.
Nîşan: Ji bo dermankirina mezinan bi hîperkolesterolemiya seretayî (heterozîgota malbatî û ne-malbatî) an bi dyslipidemia tevlihev.
Têbînî: Leqvio dermanek siRNA ye ku mRNA PCSK9 armanc dike.Ew yekem terapiya siRNA ya cîhanê ye ji bo kêmkirina kolesterolê (LDL-C).Ew bi derzîlêdana binê çermê tê rêvebirin.Derman bi navbeynkariya RNA asta proteîna PCSK9 kêm dike, bi vî rengî asta LDL-C kêm dike.Daneyên klînîkî destnîşan dikin ku ji bo nexweşên ku nikanin asta LDL-C bigihîjin asta armancê piştî dermankirinê bi dozek herî zêde ya statînan, Leqvio dikare LDL-C bi qasî 50% kêm bike.
(13)Oxlumo
Pargîdanî: Ji hêla Alnylam Pharmaceuticals ve hatî pêşve xistin.
Dema bazarê: Ji hêla Yekîtiya Ewropî ve ji bo kirrûbirrê di Mijdara 2020-an de hate pejirandin.
Nîşan: Ji bo dermankirina hîperoksaluriya seretayî ya tîp 1 (PH1).
Nîşan: Oxlumo dermanek siRNA ye ku mRNA hîdroksîsîd oxidase 1 (HAO1) dike armanc, û rêbaza rêvebirinê derzîlêdana binê çerm e.Derman bi karanîna kîmya îstîqrarê ya herî dawî ya pêşkeftî ya Alnylam, teknolojiya berhevkirina ESC-GalNAc hate pêşve xistin, ku bi domdarî û hêzek mezin siRNA-ya bi jêr çerm ve tê rêvebirin.Derman hîdroksîsîd oxidase 1 (HAO1) mRNAyê hilweşîne an asteng dike, asta glycolate oxidase di kezebê de kêm dike, û dûv re substratê ku ji bo hilberîna oxalate hewce dike vedixwe, hilberîna oxalate kêm dike da ku pêşkeftina nexweşiyê li nexweşan kontrol bike û nîşanên nexweşiyê baştir bike.
(14) Viltepso
Pargîdanî: Ji hêla NS Pharma, pargîdaniyek Nippon Shinyaku ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Tebaxa 2020-an de hate pejirandin.
Nîşan: Ji bo dermankirina dîstrofiya masûlkeya Duchenne (DMD) bi exon 53 mutasyona genê ya di gena DMD de derbas dibe.
Nîşan: Viltepso dermanek oligonukleotîdê ya antîsens e ku dikare bi pozîsyona exon 53 ya pre-mRNA ya gena DMD-ê ve girêbide, dibe sedem ku beşek ji exon 53 piştî damezrandina mRNAya gihîştî were jêbirin, bi vî rengî çarçoweya xwendina mRNA-yê bi qismî rast bike. Qutî ji nexweşan re dibe alîkar ku nîşanên ku ji hêla nexweşan ve ji hêla hin fonksiyonên proteîn ên kurtetir ve têne hevseng kirin bikin. .
(15) Amondys 45
Pargîdanî: Ji hêla Sarepta Therapeutics ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Sibata 2021-an de hate pejirandin.
Nîşan: Ji bo dermankirina dîstrofiya masûlkeya Duchenne (DMD) bi exon 45 mutasyona genê ya di gena DMD de derbas dibe.
Nîşan: Amondys 45 dermanek oligonucleotide antîsens e, oligonucleotide antîsens dikare bi pozîsyona exon 45 ya pre-mRNA ya gena DMD ve girêbide, di encamê de beşek ji exon 45 piştî damezrandina MRNAya gihîştî veqetandî tê asteng kirin, bi vî rengî beşek ji nexweşên ku fonksiyona mRNA-yê dixwîne hinekî rast dike, ji nexweşan re dibe alîkar ku fonksiyona RNA 45-ê bixwîne. proteîna normal, bi vî rengî nîşanên nexweş çêtir dike.
(16) Amvuttra (vutrisiran)
Pargîdanî: Ji hêla Alnylam Pharmaceuticals ve hatî pêşve xistin.
Dema bazarê: Ji hêla FDA ve ji bo kirrûbirrê di Hezîrana 2022-an de hate pejirandin.
Nîşan: Ji bo dermankirina amyloidosis transthyretin ya îrsî ya bi polyneuropathy (hATTR-PN) di mezinan de.
Têbînî: Amvuttra (Vutrisiran) dermanek siRNA ye ku mRNAya transthyretin (ATTR) hedef digire, ku bi derzîlêdana binavkirî tê rêvebirin.Vutrisiran li ser bingeha sêwirana platforma radestkirina konjugate ya Alnylam-a Kîmyaya Stability Enhanced (ESC)-GalNAc bi hêz û aramiya metabolîk zêde ye.Pejirandina dermankirinê li ser bingeha daneyên 9-mehî yên lêkolîna wê ya klînîkî ya Qonaxa III (HELIOS-A) ye, û encamên giştî destnîşan dikin ku terapiyê nîşanên hATTR-PN çêtir kiriye, û zêdetirî 50% ji rewşa nexweşan berevajî bûye an xirabtir bibe.
4. Dermanên din ên terapiya gene
(1) Rexin-G
Pargîdanî: Ji hêla Epeius Biotech ve hatî pêşve xistin.
Dema bazarê: Di 2005-an de, ew ji hêla Rêveberiya Xurek û Dermanê Fîlîpînê (BFAD) ve ji bo kirrûbirrê hate pejirandin.
Nîşan: Ji bo dermankirina penceşêrên pêşkeftî yên li hember kemoterapî berxwedêr in.
Têbînî: Rexin-G derziyek nanoparçikê ya bi genê barkirî ye.Ew bi vektorek retroviral genê mutant cyclin G1 dixe nav şaneyên armancê da ku bi taybetî tîmorên hişk bikuje.Rêbaza rêveberiyê înfuzyona intravenous e.Wekî dermanek tumor-armanca ku bi aktîvî li hucreyên kanserê yên metastatîk digere û wêran dike, ew li ser nexweşên ku dermanên din ên penceşêrê têk çûne, tevî biyolojîkên armanckirî, bandorek dermankirinê heye.
(2) Neovasculgen
Pargîdanî: Ji hêla enstîtuya hucreyên stem ên mirovan ve hatî pêşve xistin.
Dema navnîşkirinê: Ew di 7ê Kanûna Pêşîn, 2011-an de ji bo navnîşê li Rûsyayê hate pejirandin, û dûv re di 2013-an de li Ukraynayê hate destpêkirin.
Nîşan: Ji bo dermankirina nexweşiya damarên damarên periferîkî, di nav de iskemiya giran a lingan.
Têbînî: Neovasculgen tedawiyek genê ye ku li ser plasmîdên DNA-yê ye.Gena faktora mezinbûna endotelyal a vaskal (VEGF) 165 li ser pişta plasmîdê tê çêkirin û di nav nexweşan de tê avêtin.
(3) Collategene
Pargîdanî: Ji hêla Zanîngeha Osaka û pargîdaniyên sermayeyê ve bi hev re hatî pêşve xistin.
Dema bazarê: Ji hêla Wezareta Tenduristî, Ked û Refahê ya Japonya di Tebaxa 2019 de hate pejirandin.
Nîşan: Dermankirina iskemiya krîtîk ya lemlateya jêrîn.
Nîşan: Collategene tedawiyek genê-based plasmid e, yekem dermanê tedawiya genê ya navxweyî ye ku ji hêla AnGes, pargîdaniyek terapiya genê li Japonya ve hatî hilberandin.Hêmana sereke ya vê dermanê plasmidek tazî ye ku rêza genê ya faktora mezinbûna kezeba mirovî (HGF) vedihewîne.Ger derman di nav masûlkeyên lingên jêrîn de were derzî kirin, HGF-ya diyarkirî dê avakirina damarên xwînê yên nû li dora damarên xwînê yên girtî pêşve bibe.Lêkolînên klînîkî bandora wê li ser başkirina ulceran piştrast kiriye.
Çawa Foregene dikare alîkariya pêşveçûna terapiya genê bike?
Em di qonaxa destpêkê ya pêşkeftina dermanê siRNA de, di vekolînek mezin de, di xilaskirina dema veqetandinê de dibin alîkar.
Zêdetir hûrgulî biçin serdana:
https://www.foreivd.com/cell-direct-rt-qpcr-kit-direct-rt-qpcr-series/
Dema şandinê: Dec-27-2022